Công nghệ mô (tissue engineer) là lĩnh vực phát triển nhanh chóng gồm khoa học vật liệu sinh học, sinh học tế bào, tương tác giữa vật liệu- tế bào và các đặc tính bề mặt. Các nghiên cứu trong lĩnh vực này đều nhằm mục đích phục hồi, bảo tồn hoặc tăng cường chức năng mô đồng thời thay thế các cơ quan, mô bị tổn thương, khiếm khuyết hoặc bị mất do tai nạn hay một bệnh nào đó. Công nghệ mô liên quan tới 4 thành phần được mô tả trong Hình 1; a) các tế bào được chọn lọc và thu nhận, thông thường là tế bào gốc, b) khung sinh học (scaffold) có nguồn gốc tự nhiên hoặc ở dạng tổng hợp, c) các phân tử tín hiệu (signal molecules) như protein và các nhân tố tăng trưởng và d) bồn phản ứng sinh học (bioreactor) cung cấp môi trường sinh học cho tăng sinh và biệt hóa tế bào.
Hình 1: Bốn thành phần chính của công nghệ mô (Nguồn: http://www.ncbi.nlm.nih.gov/).
Mô hoặc cơ quan có thể tạo thành thông qua một số phương pháp, trong đó phương pháp phổ biến nhất liên quan tới thu nhận các tế bào đặc hiệu mô từ mẫu sinh thiết mô nhỏ của bệnh nhân và thu nhận bằng nuôi cấy invitro. Các tế bào thu nhận sau đó được tăng sinh và cấy vào khung 3D (three-dimension scaffold) có cấu trúc bắt chước chất nền ngoại bào (extracellular matrices-ECM, có tác dụng ổn định cấu trúc tế bào và thực hiện một số chức năng khác) của mô mục tiêu. Chức năng chính của scaffold là 1) đưa các tế bào vào các vị trí mong muốn trong cơ thể bệnh nhân, 2) kích thích tương tác giữa tế bào – vật liệu sinh học, c) tăng cường sự bám dính tế bào, 3) cho phép vận chuyển đầy đủ oxygen, chất dinh dưỡng và các nhân tố tăng trưởng đề đảm bảo tế bào tồn tại, tăng sinh và biệt hóa, 4) kiểm soát cấu trúc và chức năng của mô được tạo ra. Tế bào được đưa vào scaffold, sau đó cấy ghép vào cơ thể bệnh nhân bằng cách tiêm trực tiếp hoặc cấy mô vào vị trí mong muốn trên cơ thể người bệnh bằng phương pháp phẫu thuật (Hình 2).
Hình 2: Sơ đồ minh họa phương pháp công nghệ mô phổ biến nhất, trong đó các tế bào đặc hiệu được thu nhận từ bệnh nhân, tăng sinh invitro, cấy vào scaffold và sau đó chuyển vào cơ thể bệnh nhân (Nguồn: http://www.ncbi.nlm.nih.gov/).
“Chúng tôi đã làm việc trên hệ thống in này khoảng 10 năm với mục tiêu chính là tạo ra cấu trúc ở người”, theo tiến sĩ Anthony Atala, Viện Wake Forest. “Tự nhiên có giới hạn tự nhiên về mặt khoảng cách khuếch tán, do vậy một phần của thách thức trong lĩnh vực này là tạo ra con đường dẫn trong mô nhằm mục đích cho phép các chất dinh dưỡng có thể tiếp cận các tế bào nằm sâu bên trong mô”.
Hệ thống ITOP có 3 thành phần chính: (1) bệ điều khiển 3 trục X, Y, Z được kết nối với máy tính; (2) bộ phận phân phối tế bào gồm nhiều ống (cartridge) và bộ phẩn kiểm soát khí (pneumatic controller); (3) hộp kín có bộ kiểm soát nhiệt độ và độ ẩm là nơi thực hiện quá trình in mô. Hệ thống ITOP sử dụng chương trình trên máy tính để tạo ra danh sách lệnh cho sự di chuyển của bệ XYZ (hình 3a). Để tiến hành in mô, Atala và cộng sự đã chuyển đổi dữ liệu lâm sàng từ hình ảnh chụp cắt lớp CT (computed Tomography) và MRI (Magnetic resonance imaging) vào bộ phận thiết kế có kết nối với máy tính. Sau đó họ tạo ra một chương trình hướng dẫn các ống của máy in chứa tế bào trong các trục XYZ và kiểm soát áp suất không khí (Hình 3c).
Hình 3: a) cấu trúc hệ thống in mô- cơ quan ITOP, b) cấu trúc in 3D, c) quy trình in mô sử dụng hệ thống ITOP ()
Để giữ các tế bào lắng, nhóm nghiên cứu của Atala đã tạo ra hydrogel đóng vai trò scaffold gồm fibrinogen (tăng cường độ ổn định của cấu trúc và tạo ra vi môi trường giúp các tế bào bám chặt và tăng sinh), gelatin (có đặc tính đông đặc và hóa lỏng tại các nhiệt độ thích hợp), hyaluronic acid (HA) và glycerol (cả hai đều tạo ra kết cấu chuẩn xác cho scaffold).
Hydrogel là một loại mực in sinh học (bioink) phổ biến được dùng trong công nghệ mô, có thể ở dạng tự nhiên hoặc tổng hợp. Hydrogel được sử dụng phổ biến trong quá trình in sinh học, giúp ổn định các tế bào và bắt chước môi trường chất nền ngoại bào (extracellular maitrix-ECM) giúp tế bào phát triển và có tính linh động tương tự các mô tự nhiên. Một số hydrogel thường được sử dụng trong công nghệ in mô và cơ quan gồm alginate, collagen, gelatin, methacrylate, hyaluronic acid, fibrin, polyethanol glycol và pluronic F127. Trong quá trình in cơ quan 3D, các tế bào sẽ được đưa vào các lớp hydrogel theo thứ tự tạo lớp hydrogel, đưa tế bào vào trong, sau đó lại tạo một lớp hydrogel và quá trình tiếp tục cho đến khi hoàn thành quá trình in.
Nhìn chung, hydrogel sử sụng trong công nghệ in 3D cần đạt các tiêu chuẩn sau: 1) không độc, 2) ổn định hình dạng của cấu trúc được in và hình thái bên trong sau quá trình lắng đọng (deposition), 3) có tính ổn định và các đặc tính hóa học phù hợp cho nuôi cấy invitro và quá trình cấy ghép invivo, 4) bảo đảm khả năng sống sót và chức năng của tế bào, 5) dễ thao tác. Ngoài ra, hydrogel cần phải cung cấp cho các tế bào được cấy vào sự kích thích sinh hóa và vật lý phù hợp để dẫn dắt các quá trình tế bào khác nhau như sự di chuyển của tế bào, tăng sinh và biệt hóa.
Các ống của máy in chuyển các tế bào vào hydrogel được thêm polymer PCL (poly-caprolactone) vào cấu trúc bên trong, và Pluronic f127 (đường gờ bên ngoài được loại bỏ ngay khi quá trình in hoàn thành). Các vi kênh (microchannel) dạng lưới giữa các tế bào cho phép oxy và các chất dinh dưỡng có thể di chuyển đến tất cả các tế bào. Các mô được in sau đó bắt đầu tiết chất nền (matrix) của chính nó đồng thời scaffold tạm thời sẽ bị phân hủy.
Bằng cách này, các nhà nghiên cứu đã tạo ra mảnh xương hàm dưới dùng các tế bào gốc thu nhận từ dịch nước ối ở người. Đồng thời tạo ra thành công xương sọ chuột và sau đó cấy mô này vào chuột. Sau 5 tháng thực hiện cấy ghép, mạch máu mới đã được hình thành trong mô cấy.
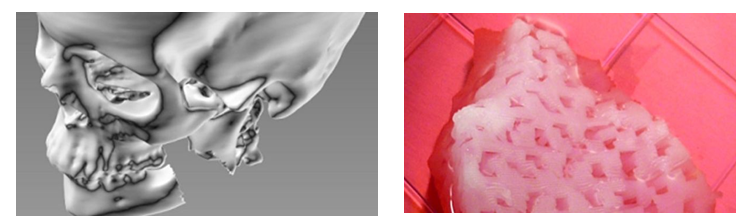
Theo tiến sĩ Atala, “Chúng tôi tiến hành chụp hình xương quai hàm của bệnh nhân, sau đó chuyển dữ liệu hình ảnh vào phần mềm của máy in để tạo ra mảnh xương hàm bị vỡ cho bệnh nhân” (Hình 4).
Hình 4. Hình chụp xương hàm bị vỡ và mô thay thế được tạo ra từ công nghệ in 3D (Nguồn: http://www.bbc.com/)
Không những thế, Atala và cộng sự còn tạo ra nhiều mô có cấu trúc phức tạp hơn, chẳng hạn cấu trúc tai người từ tế bào sụn (chondrocyte) thu nhận từ tai thỏ và cơ xương dùng nguyên bào cơ (myoblast) chuột. Khi cấy vào chuột, các cơ được tạo ra từ công nghệ in này có đáp ứng thích hợp với sự kích thích điện.
Cho đến nay, nhóm nghiên cứu đã tạo ra một số máy in sinh học này. “Các thiết bị này là chiến lược chúng tôi muốn phổ biến để những nhà khoa học khác cũng có thể dùng nó”, theo Atala, “Chúng tôi muốn các công nghệ này có thể dùng để điều trị cho bệnh nhân ngay khi có thể”.
Ngoài ra, công nghệ in mô, cơ quan 3D còn giúp lập kế hoạch trước trong các quy trình phẫu thuật phức tạp. Các bác sĩ và bệnh viện khắp nơi trên thế giới bắt đầu chú ý đến công nghệ in cơ quan 3D sau nhiều cuộc phẫu thuật ứng dụng công nghệ này thành công. Bản sao cơ quan in 3D không chỉ giúp bệnh nhân có hiểu biết chính xác hơn về bệnh của họ mà còn giúp cho bác sĩ có thể đưa ra kế hoạch phẫu thuật trước khi thực hiện trên cơ thể bệnh nhân, do đó giảm thời gian và tăng độ chính xác trong ca phẫu thuật. Các bác sĩ Trung Quốc đã ứng dụng công nghệ này để thực hiện các ca phẫu thuật phức tạp như tách rời cặp song sinh dính liền nhau, phẫu thuật não để cứu bệnh nhân nữ 50 tuổi hay sửa lại quai hàm cho bé gái 3 tuổi. Gần đây, họ cũng đã thực hiện thành công phẫu thuật mở tim trên bệnh nhân chỉ chín tháng tuổi có khiếm khuyết ở tim dùng công nghệ in 3D để tạo ra mô hình tim, từ đó lên kế hoạch phẫu thuật cho bệnh nhân.
Tài liệu tham khảo:
http://www.bbc.com/news/health-35581454
https://3dprint.com/124954/3d-printed-heart-saves-baby/
http://iopscience.iop.org/article/10.1088/1758-5090/8/1/015007
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3963751/
http://www.rsc.org/images/loc/2012/pdf/M.3.100.pdf
http://www.nature.com/ncomms/2014/140602/ncomms4935/pdf/ncomms4935.pdf